

24小時服務熱線: 認證谘詢:13516989992 檢測谘詢:13362910005 0579-85573858
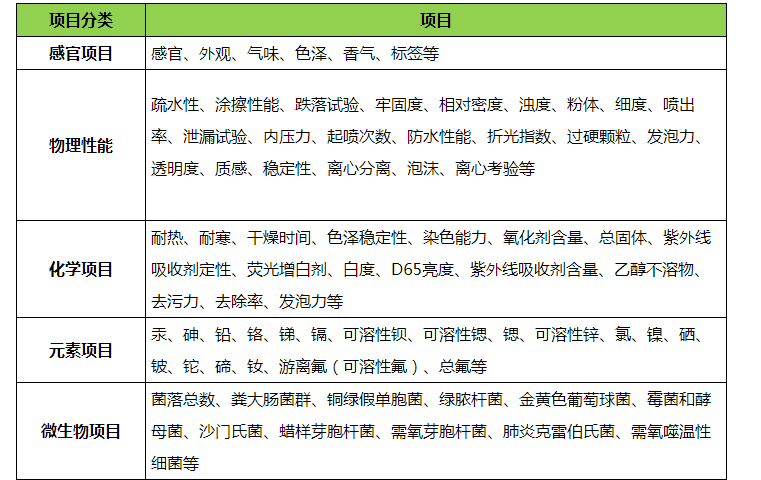
隨著人們生活水平的提高,化(huà)妝品逐步進入了我們的生活,日(rì)常生活中我們人人都會與化妝品接觸。由於(yú)我們的使用頻率較高,所以化妝品的質量好壞會影響我們的身體健康,我們需(xū)要重視。化妝品檢測主要是關注重金屬、微生(shēng)物(wù)、抗生素、激素、毒理、抗生素、標準(zhǔn)禁止(zhǐ)添加項目等。
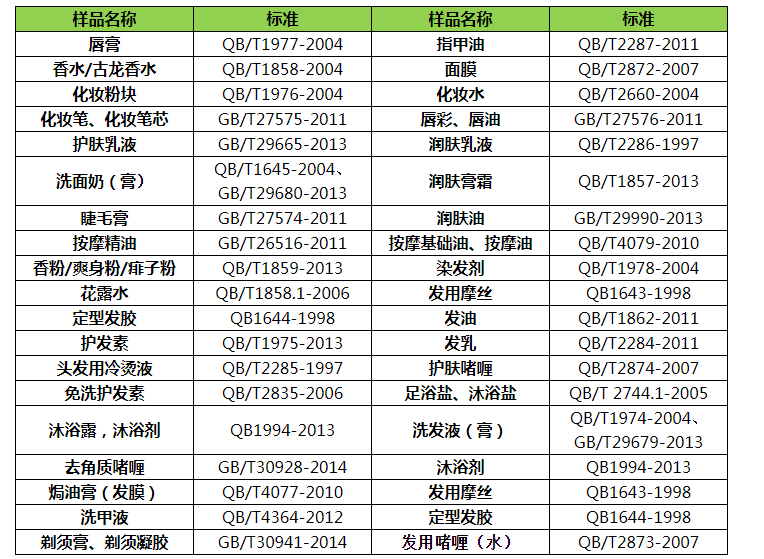
範圍:
清潔類:牙膏、洗麵(miàn)奶(膏)、洗發液(膏)、香皂、足
浴鹽/沐浴(yù)鹽、沐(mù)浴劑等
護膚類:潤膚乳液、潤膚膏霜等
滋養(yǎng)類:化妝水、麵膜、護發素、發乳、發油等
美容類:化妝粉塊、唇膏、香水/古龍水、香粉/爽身粉/痱子粉、定型發膠、發用摩絲、染發劑花露水、指甲油等

化妝品非特(tè)備案
特殊用(yòng)途化妝(zhuāng)品分別是:育發、染發、燙發、脫毛(máo)、美(měi)乳、健(jiàn)美、除臭、祛斑和防曬9類化妝品,除此之外的化妝品叫做(zuò)非特殊用途(tú)化妝品,也就是普通化妝品。
一、凡在中華人民共和國境內生產的非特殊用途化妝品,生產企業應按本規(guī)定要求進行產品信息備案。
二、生產企業應當在產品(pǐn)上市銷售前(qián),將產品配方(不包括含量,限用物質除外)及銷售包裝(含產(chǎn)品標簽、產品說明書)的(de)信息按要求(qiú)通過統一的網絡平台報(bào)送至所在行政區域內的省級(jí)食品藥品監管部門。產品(pǐn)安全性評估(gū)資料、產品生產工藝簡(jiǎn)述、產品(pǐn)生產設備(bèi)清單(dān)、產品技術要求及產品檢驗(yàn)報告等資料由生產企業妥(tuǒ)善保存備查。
三、委托生(shēng)產(chǎn)的(de)產品,委托雙方應分別向所在行政區域內的(de)省級食品藥品監督管理部門報送備案信(xìn)息。僅供出口(kǒu)的,由實際生產企業向所在(zài)行政區域(yù)內的省級食品藥品監督管理部門報送備案信(xìn)息。
四、省級食品藥品監督管理部門收到企業的備案信息後,應當在5個(gè)工作日內完成對備案資料完整性(xìng)的核查。符合(hé)要求的,通過國家食品藥品監管總局(jú)政務網公布產(chǎn)品備案信息,供公眾查詢。
五、對於不屬於(yú)備(bèi)案產品範圍的、備案資料不齊全或(huò)備案資料不符合規定形式的,省級食(shí)品藥品監督管理(lǐ)部門應在(zài)5個工作日內告知企業並說明理由。存在明顯違法(fǎ)情形的,應當責令立即改正,不得(dé)上市銷售。
六、省級食品藥品監督部門應(yīng)當在備案後(hòu)三個月內(nèi)組織開展對備案產品的實質審查,發現不符合國家相關規定的(de),應當依法予以查處。
七、已經備案的產品,擬變更原(yuán)備案事項的(de),應在變更前將相關(guān)變更信息報送備案。涉及備案管理部門改變的,應主動申請注(zhù)銷原(yuán)備案信息後,直接申請重新備案。
八、已獲備案的產品,自備案之日起每滿(mǎn)4年應重新按本規定要求提交產品備案信息(xī)。
九、產品配方信息的報送應符合以下要求:
1.全(quán)部原料(liào)應詳細列明標準中文名稱、原料序號、限用物質含量、使用目的等內容。
2.複配原料應以複配形式填報,應標明各組分的標準中(zhōng)文名稱。香精不須列明具體香料組分(fèn)的種類和含量。
3.原料(含複配原料中的各組分)應按《國際(jì)化妝(zhuāng)品原料標準中文名稱目錄》使用標準中文(wén)名稱,無(wú)國際化(huà)妝品原料名稱(INCI)或未列入《國際(jì)化妝品原料標準(zhǔn)中文名稱目錄》的,應使用《中國藥典(diǎn)》中的名稱或化學名稱或植物拉丁學名,不得使用商品名或俗名,但複配原料除外。
4.著(zhe)色劑應提供《化妝品衛生規範》中載明的著(zhe)色劑索(suǒ)引(yǐn)號(簡稱CI號),無CI號的除外。
5.凡在產品配方中使用(yòng)來源於石油、煤焦油的碳氫化合物的(單一組分的除外),應標明相關原料的化學文摘索引號(簡(jiǎn)稱CAS號)。
6.使(shǐ)用動物髒器組(zǔ)織及血(xuè)液製品提取物的原料,應當收集該原料的來源、質(zhì)量(liàng)規格和原料生產國允許使用的證明等資料存檔(dàng)備查。
7.使用《化妝品衛生規範》對限用物質有規格要求的原料,應當收集該原料(liào)生產商出具的原料質量規(guī)格證明存檔備查(chá)。
8.宣(xuān)稱為兒(ér)童或嬰兒使用的產品,配方設計原則(含配方整體分析報告)、原料的選(xuǎn)擇原則和要(yào)求、生產工藝、質量控製等內容(róng)應(yīng)當(dāng)按照《兒童化妝(zhuāng)品申報與審評指南》(國食藥(yào)監保化[2012]291號)的(de)要求編(biān)製,相關資料應當存檔備查。
9、產品技術要求的編製參照《關於印發化妝品產品技術要求規範的通知》(國食藥監許[2010]454號(hào))要求執行;檢驗要求(qiú)參照《關於印發化(huà)妝品行政(zhèng)許可檢驗管理辦法的通知》(國食藥監許[2010]82號)執行,其中企業參照《關(guān)於印發化妝品中可能存在(zài)的安全性風險物質風險評估(gū)指南的通知》(國食藥監許[2010]339號)要求進行風險評估(gū)並確認產品安全性(xìng)的,可免做毒理相關檢測。
浙江和諾檢測技術有限公司可以提(tí)供樣品送檢服務,進行(háng)非特備案的谘詢和指導。
歐盟CPSR(化妝品安全報告)
CPSR(化妝品安全報(bào)告)是(shì)產品進入歐盟市場的通行證,歐盟化妝品新法規Regulation(EC)1223/2009已於(yú)2013年7月11日正式實施,相比(bǐ)於之前的化(huà)妝品指令Directive 76/768 EEC,對化妝品的安全性提出了更加嚴格的要求,其中明(míng)確規定了產品必須完成化妝品安(ān)全報(bào)告(gào)(Cosmetic Product Safety Report,CPSR)後方能夠在歐盟經濟區上市銷售。
根據新法規(guī),歐洲化妝品協會(原Colipa)和歐(ōu)盟委員會共同製定了化(huà)妝品安全報告指南,詳細(xì)解讀(dú)和列出了法(fǎ)規中(zhōng)關於CPSR的要求。該指南文件於(yú)2013年11月 25日由歐盟委(wěi)員會作為委員(yuán)會(huì)決議(Commission Decision)發布,歐盟委員會決議具有法律效率,因(yīn)此企業必須(xū)遵從該決議。目前進行的毒理學風險評估(Toxicological Risk Assessment,TRA)以及類似(sì)的簡單升級版本已經(jīng)不能夠滿足(zú)CPSR以及該指南的(de)要求。指南更加細化了新法規關(guān)於CPSR的要求。增(zēng)加的重要細則如下:
1. 產品配方(fāng)中的各組分需提供準確的含量,若(ruò)無(wú)法提供定量信息則按照(zhào)高劑量計算。複雜成分如提取物(wù)或生物製品等需提供純度標準及測試方法。
2. 產品中使用的原材料供(gòng)應商(shāng)須在報(bào)告中指出,香料(liào)和香精必須提供(gòng)生產商和產品(pǐn)代碼信息。
3. 化妝品包裝材料需要滿足食品接觸材料(liào)(Food Contact Material)的標準並保證其穩定(dìng)性。特別對於一些對光和空氣敏感的產品,其(qí)正(zhèng)確的貯存(cún)方法需要在標簽上(shàng)得以體現(xiàn)。
4. 產品需要提供穩定性(Stability)報告,其(qí)中包括穩定性測定方法,防腐劑(jì)挑戰試驗報(bào)告,產(chǎn)品有效期以及開蓋使用(yòng)日期(Period-after-opening)。
5. 化妝品微生物方麵的要求進一步細化(huà),高風險的原料需要注意微生物危害。
6. 化妝品原料以及(jí)其包材(cái)中可(kě)能含有的雜質需(xū)要進(jìn)行(háng)風險評估並(bìng)證明其技術上(shàng)是不可避免的(如GMP條(tiáo)件下也(yě)無法避免)。
7. 化(huà)妝品所使(shǐ)用(yòng)的原料(liào)需要提(tí)供詳細的毒理檔案(Toxicological Profile of Substance,TPS),每一個原料需要提供其(qí)毒理學信息,包括急性毒性、刺激性、過敏(mǐn)性等(děng)共12項(xiàng)毒理學端點。
8. 化妝品原材料和成品的生產商都需要達(dá)到GMP(ISO 22716)標準。 由於原料中的雜質具有潛在的可以影響(xiǎng)物質毒性的風險因素,因此在評估雜質的安全性時可以引(yǐn)入毒理學(xué)關(guān)注(zhù)閾值(TTC)作(zuò)為有效(xiào)的評估手(shǒu)段(duàn)。
9. 若出現不良反應(yīng),則需在報告中(zhōng)評估其發生的可能性和因果關係,出現(xiàn)嚴重的不良反應需上報歐盟成(chéng)員國有關主管部門,並在CPSR報告中以附件形式存在並描述處理和解決方法。
10. 在評估報告結論中必須提到新的化妝品法規Regulation(EC)1223/2009,並且明確指出(chū)產品是否(fǒu)符合新的化妝(zhuāng)品法規。
11. 關於產品標簽,警(jǐng)告用語和使用說明在滿足新法規外還須參考相關文件,如 Commission Recommendation 2006/647/EC 及其它與標(biāo)簽相關的指導文件。為了直觀地表達該內容,可以在CPSR中附上產品的圖片。
12. 毒(dú)理風險評估由定性評估變(biàn)為定量評估。包括產品係統性的(de)風險評(píng)估,配方組合後的兼容性,穩定性(xìng),微生物,包裝,標簽以及使用等各個方麵。產品(pǐn)所有的測試(shì)報告(gào)、技術文檔和其它相關信息須(xū)經過毒理風險(xiǎn)評估師評估(gū),並特別注意三歲以下兒童使用的產品(pǐn),除了滿足新法規要求(qiú)還需遵循歐盟消費者安全科學委員會(SCCS)指南。
13. 當法(fǎ)律要求出現變化或更改時,產品的原材(cái)料發生改變(如更換供應商),使用條件發生改變,以及監測到在正常使用條件下不良反應發(fā)生率增加時,毒理風險評估師須對產品進行重新評估,確保化妝品安全報告(CPSR)保持同步(bù)更新並滿足新法規要求。
14. 指南對於可以出具化妝品(pǐn)安全報告(CPSR)的安全評估師資質做(zuò)了詳細的(de)定義,非(fēi)歐盟成員國承認的藥學,毒理學等相(xiàng)關專業人員不得從事化妝品(pǐn)安全報告評估工作。並(bìng)且評估師的資質及相(xiàng)關學曆證明需要附在評估報告後(hòu)。
相關信息/ RELATED INFO
MORE
服(fú)務熱線
微信掃(sǎo)一掃


返回頂部